今回を含めて4回にわたって、二次電池技術について解説する。今回は「電池について」、次回以降に「リチウムイオン電池について」「大容量蓄電池システムの利用」「二次電池への期待」を紹介する。二次電池は、種々の電極材料で、多種多様な組み合わせで構成できる。実用化には、充放電の繰り返し回数の多さ、軽量・コンパクト、ノーメンテナンス、低コストに加えて、高安全性が求められる。「二次電池」は、低炭素、情報社会のキーテクノロジーである。
電池の始まりは紀元前。近代の開発史に日本の貢献は大きい
電池の始まりは、紀元前のバクダットの遺跡から出土したワインビネガーの入った容器という説もある。メッキに使っていたようだ。
有史では、1791年にイタリアでガルバニがカエルの解剖でガルバニ電流を発見し、発表した。その直後、1800年には、ボルタが、正極に亜鉛版、電解液に硫酸水溶液、負極に銅版を用いたボルタ電池を発明した。
日本に目を向ければ、1887年に屋井先蔵が「乾電池」を発明し、日清戦争で利用された。1897年には、島津源蔵(二代目)が鉛電池を日本で初めて製造。1920年には酸化鉛の効率的な製造方法を考案した。GSユアサでは、現在も、空気中で金属鉛を回転機によってゴロゴロと粉砕するこの手法が用いられている。鉛蓄電池は長年の実績があり、現在も、自動車をはじめ、ビルの消防設備やバックアップ電源に使われている。
一方、吉野彰先生のノーベル賞受賞もあり注目されたリチウムイオン電池は、1990年代に市販が始まったもので、スマートフォンなどの携帯機器から電気自動車、さらに近年では電力貯蔵にも利用されている。日常生活に欠かせないアイテムである。
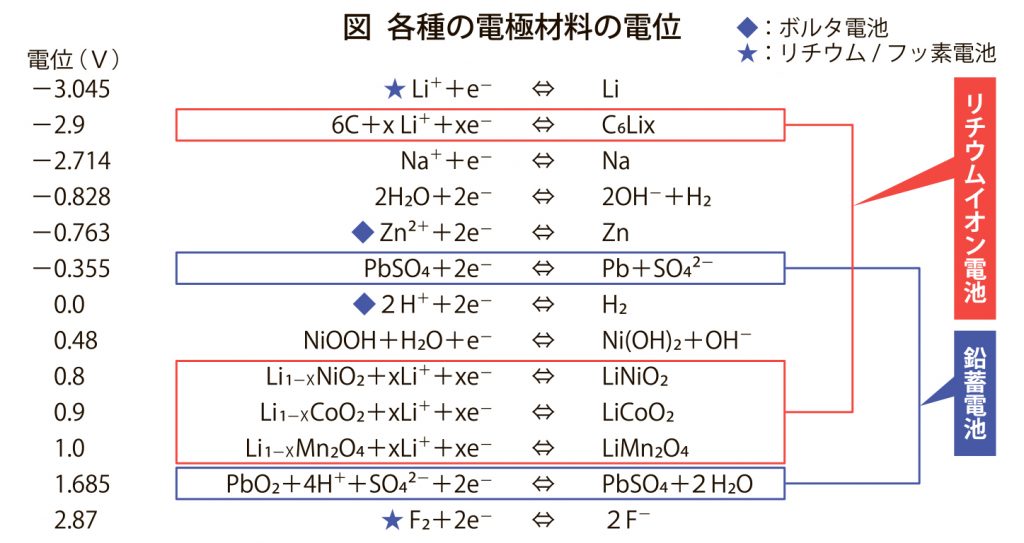
電池は、2種類の異なる材料間でイオンと電子がそれぞれの経路で移動すれば構成できる=図。例えば、ボルタ電池では、正極の金属亜鉛が硫酸水溶液中に溶け出して、負極の銅表面での水素発生により放電する。また、鉛蓄電池は、二酸化鉛/硫酸/鉛の組み合わせで、約2Vの電圧で動く。究極の電池は、リチウム金属(負極)/フッ素(正極)の組み合わせで、作動電圧5Vを超えるはずである。ただし、まだ夢の電池である。
二次電池は多種・多様な構成が可能
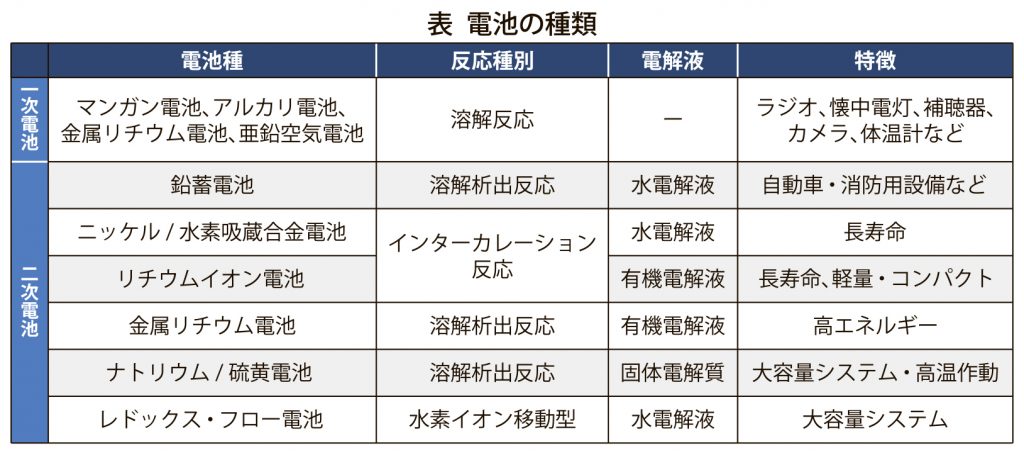
電池には、大別して、一次と二次がある。放電のみの、使いきりの電池が一次電池である。充電・放電して、何回も繰り返し使えるのが二次電池である。一次電池は、繰り返し使用することを想定した構造になっていないため、充電は“絶対に禁物”である。
二次電池は、さらに、充電・放電に伴う反応により「溶解析出型」と「インターカレーション型」反応の2種類に分けられる=表。ニッケル/亜鉛電池や鉛蓄電池は、溶解析出反応のため、電極形状の維持が難しく、長期間のサイクル運転に課題が残る。一方、リチウムイオン電池やニッケル水素電池は、材料の結晶中にある空間にイオンが出入りするインターカレーション反応によるため、電極内で活物質の形状が維持しやすく、長期間でのサイクル運転が期待できる。
また、電解質では、大きく3つ、水溶液系電解液と有機電解液、さらに、固体電解質で分けられる。有機電解液は、電気分解の耐電圧が高いため、作動電圧を高くできる。水電解液では、水の電気分解をさせる必要があるために、作動電圧が低くなる。固体電解質では、さらに、耐電圧が高く、高電圧化が期待できる。
二次電池は、正負極の電極材料、電解液の組み合わせで、多種多様な電池を構成できる。しかし、実用化には、繰り返し使用できる回数の多さ、軽量・コンパクト、ノーメンテナンス、低コスト、さらには、安全性の確保が求められる。リチウムイオン電池は高性能ではあるが、利用分野の拡大には、さらなる高安全化が求められている。
電気新聞2020年6月22日
















